Este articulo hace referencia de los Flaminoides en el S. Cardio vascular, por eso también es importante para persona que sufren S.Q.M., pues de cualquiera manera pueden beneficiarse de las propiedades de los flaminoides
Los flavonoides como terapia antioxidante.
Dr. Ricardo O. Russoa y Dr. Mario Speranza Sánchezb
Revista Costarricense Cardiologia
Dr. Ricardo O. Russoa y Dr. Mario Speranza Sánchezb
Revista Costarricense Cardiologia
Introducción
En la revisión de Martínez-Flórez et al acerca de las propiedades y acciones antioxidantes de los flavonoides, se refiere que estos compuestos fueron descubiertos por el premio Nobel Szent-György, quien en 1930 aisló una sustancia de la cáscara del limón denominada citrina, con acción modificadora de la permeabilidad capilar. Los flavonoides primero atrajeron el interés de los farmacólogos cuando se describieron sus propiedades similares a las vitaminas, por tal motivo se designaron como vitamina P (por permeabilidad) y también vitamina C2 (porque algunos tenían propiedades análogas a la vitamina C). Sin embargo, como no fue posible confirmar que estas fueran vitaminas, ambas designaciones se dejaron de usar alrededor de 1950.
En la revisión de Martínez-Flórez et al acerca de las propiedades y acciones antioxidantes de los flavonoides, se refiere que estos compuestos fueron descubiertos por el premio Nobel Szent-György, quien en 1930 aisló una sustancia de la cáscara del limón denominada citrina, con acción modificadora de la permeabilidad capilar. Los flavonoides primero atrajeron el interés de los farmacólogos cuando se describieron sus propiedades similares a las vitaminas, por tal motivo se designaron como vitamina P (por permeabilidad) y también vitamina C2 (porque algunos tenían propiedades análogas a la vitamina C). Sin embargo, como no fue posible confirmar que estas fueran vitaminas, ambas designaciones se dejaron de usar alrededor de 1950.
¿Qué son los flavonoides?
Los flavonoides son compuestos fenólicos de 15 carbonos, que se distribuyen en el reino vegetal en más de 2.000 especies de muy diversas familias. Desempeñan un papel importante en la fisiología vegetal, dado que responden a la luz y controlan los niveles de las auxinas reguladoras del crecimiento y diferenciación de las plantas2. En su estructura química contienen un número variable de grupos hidro-fenólicos, son quelatantes del hierro y otros metales de transición y presentan una gran capacidad antioxidante que depende de las propiedades redox de sus grupos hidroxifenólicos y de la acción inhibitoria de radicales hidroxilo y superóxido, altamente reactivos en la cadena de peroxidación lipídica3,4.
También se ha referido su capacidad de prevenir la agregación plaquetaria4 (efectos antitrombóticos) y de proteger a las lipoproteínas de baja densidad de la oxidación5 (prevención de la placa de ateroma). Además, otros autores han encontrado que tienen efectos terapéuticos en un elevado número de condiciones patológicas, incluyendo la aterosclerosis y la cardiopatía isquémica6,7,8,9.
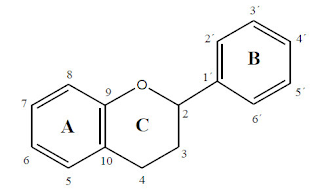
Químicamente, los flavonoides son compuestos de bajo peso molecular que comparten un esqueleto común de difenilpiranos (C6-C3-C6), compuesto por dos anillos de fenilos (A y B) ligados a través de un anillo C de pirano (heterocíclico). Los átomos de carbono en los anillos C y A se numeran del 2 al 8,
y los del anillo B desde el 2’ al 6’10, 11. (figura 1). Esta estructura básica permite una multitud de patrones de sustitución y variaciones en el anillo C.
Los flavonoides son compuestos fenólicos de 15 carbonos, que se distribuyen en el reino vegetal en más de 2.000 especies de muy diversas familias. Desempeñan un papel importante en la fisiología vegetal, dado que responden a la luz y controlan los niveles de las auxinas reguladoras del crecimiento y diferenciación de las plantas2. En su estructura química contienen un número variable de grupos hidro-fenólicos, son quelatantes del hierro y otros metales de transición y presentan una gran capacidad antioxidante que depende de las propiedades redox de sus grupos hidroxifenólicos y de la acción inhibitoria de radicales hidroxilo y superóxido, altamente reactivos en la cadena de peroxidación lipídica3,4.
También se ha referido su capacidad de prevenir la agregación plaquetaria4 (efectos antitrombóticos) y de proteger a las lipoproteínas de baja densidad de la oxidación5 (prevención de la placa de ateroma). Además, otros autores han encontrado que tienen efectos terapéuticos en un elevado número de condiciones patológicas, incluyendo la aterosclerosis y la cardiopatía isquémica6,7,8,9.
Químicamente, los flavonoides son compuestos de bajo peso molecular que comparten un esqueleto común de difenilpiranos (C6-C3-C6), compuesto por dos anillos de fenilos (A y B) ligados a través de un anillo C de pirano (heterocíclico). Los átomos de carbono en los anillos C y A se numeran del 2 al 8,
y los del anillo B desde el 2’ al 6’10, 11. (figura 1). Esta estructura básica permite una multitud de patrones de sustitución y variaciones en el anillo C.
¿Cómo se clasifican los flavonoides?
En función de sus características estructurales los flavonoides se pueden clasificar en:
1. Flavanos, como la catequina, con un grupo -OH en posición 3 del anillo C.
2. Flavonoles, representados por la quercitina, que posee un grupo carbonilo en posición 4 y un grupo -OH en posición 3 del anillo C.
3. Flavonas, como la diosmetina, que poseen un grupo carbonilo en posición 4 del anillo C y carecen del grupo hidroxilo en posición C3.
4. Antocianidinas, que tienen unido el grupo -OH en posición 3 pero además poseen un doble
En función de sus características estructurales los flavonoides se pueden clasificar en:
1. Flavanos, como la catequina, con un grupo -OH en posición 3 del anillo C.
2. Flavonoles, representados por la quercitina, que posee un grupo carbonilo en posición 4 y un grupo -OH en posición 3 del anillo C.
3. Flavonas, como la diosmetina, que poseen un grupo carbonilo en posición 4 del anillo C y carecen del grupo hidroxilo en posición C3.
4. Antocianidinas, que tienen unido el grupo -OH en posición 3 pero además poseen un doble
Figura 1. Estructura básica de los flavonoides. enlace entre los carbonos 3 y 4 del anillo C.
Según Martínez-Flórez et al existen tres característicasestructurales que son importantes para su función:
a. La presencia en el anillo B de la estructura catecol u O-dihidroxi;
b. La presencia de un doble enlace en posición 2,3; y
c. La presencia de grupos hidroxilo en posición 3 y 5. La quercitina presenta las tres características, mientras que la catequina solo presenta la segunda y la diosmetina la primera (figura 2).
a. La presencia en el anillo B de la estructura catecol u O-dihidroxi;
b. La presencia de un doble enlace en posición 2,3; y
c. La presencia de grupos hidroxilo en posición 3 y 5. La quercitina presenta las tres características, mientras que la catequina solo presenta la segunda y la diosmetina la primera (figura 2).
Fuentes naturales
Los flavonoides se encuentran en productos que son consumidos en la dieta humana de forma habitual tales como frutas, verduras y semillas, así como en bebidas como té verde, té negro, cerveza y vino así como en forma de suplementos nutricionales, junto con ciertas vitaminas y minerales12,13,14.
El vino tiene un alto contenido en compuestos polifenólicos, aproximadamente se conocen unos 500, la mayoría de los cuales provienen de la uva y del proceso fermentativo. En la uva estas moléculas se localizan en la piel, especialmente en las células epidérmicas, y en las pepitas. Su cantidad y tipo depende principalmente de la variedad de la vid, del clima, del terreno y de las prácticas de cultivo15. La cerveza también contiene importantes cantidades de flavonoides entre los que destacan los polihidroxiflavanos (catequiza y epicatequina), los antocianógenos (leucocianidina o leucopelargonidina) y los flavonoles (grupo de quercitinas: kaempferol o mirecitina15).
La ingesta promedio de flavonoles y flavonas se sitúa entre los 20 y 26 mg/día16,17.
Se han identificado más de 5.000 flavonoides18, entre los que se pueden destacar:
1. Citroflavonoides: quercitina, hesperidina, rutina, naranjina y limoneno. La quercitina es un flavonoide amarillo-verdoso presente en cebollas, manzanas, brócoli, cerezas, uvas o repollo rojo. La hesperidina se encuentra en los hollejos de las naranjas y limones. La naranjina da el sabor amargo a frutas como la naranja, limón y toronja, y el limoneno se ha aislado del limón y la lima.
2. Flavonoides de la soya o isoflavonoides: están presentes en los alimentos con soya tales como frijoles, leche, harina y proteína vegetal texturizada. Los dos más conocidos son la genisteína y la daidzeina.
Los flavonoides se encuentran en productos que son consumidos en la dieta humana de forma habitual tales como frutas, verduras y semillas, así como en bebidas como té verde, té negro, cerveza y vino así como en forma de suplementos nutricionales, junto con ciertas vitaminas y minerales12,13,14.
El vino tiene un alto contenido en compuestos polifenólicos, aproximadamente se conocen unos 500, la mayoría de los cuales provienen de la uva y del proceso fermentativo. En la uva estas moléculas se localizan en la piel, especialmente en las células epidérmicas, y en las pepitas. Su cantidad y tipo depende principalmente de la variedad de la vid, del clima, del terreno y de las prácticas de cultivo15. La cerveza también contiene importantes cantidades de flavonoides entre los que destacan los polihidroxiflavanos (catequiza y epicatequina), los antocianógenos (leucocianidina o leucopelargonidina) y los flavonoles (grupo de quercitinas: kaempferol o mirecitina15).
La ingesta promedio de flavonoles y flavonas se sitúa entre los 20 y 26 mg/día16,17.
Se han identificado más de 5.000 flavonoides18, entre los que se pueden destacar:
1. Citroflavonoides: quercitina, hesperidina, rutina, naranjina y limoneno. La quercitina es un flavonoide amarillo-verdoso presente en cebollas, manzanas, brócoli, cerezas, uvas o repollo rojo. La hesperidina se encuentra en los hollejos de las naranjas y limones. La naranjina da el sabor amargo a frutas como la naranja, limón y toronja, y el limoneno se ha aislado del limón y la lima.
2. Flavonoides de la soya o isoflavonoides: están presentes en los alimentos con soya tales como frijoles, leche, harina y proteína vegetal texturizada. Los dos más conocidos son la genisteína y la daidzeina.
3. Proantocianidinas se localizan en las semillas de uva y vino tinto
4. Antocianidinas: son pigmentos vegetales responsables de los colores rojo y rojo-azulado de las cerezas.
5. Ácido elágico: se encuentra en frutas como la uva y en verduras.
6. Catequina: en té verde y negro.
7. Kaemferol: aparece en puerros, brócoli, rábano y remolacha
4. Antocianidinas: son pigmentos vegetales responsables de los colores rojo y rojo-azulado de las cerezas.
5. Ácido elágico: se encuentra en frutas como la uva y en verduras.
6. Catequina: en té verde y negro.
7. Kaemferol: aparece en puerros, brócoli, rábano y remolacha
Metabolismo de los flavonoides
La transformación de los flavonoides ocurre en el hígado, por medio de reacciones de biotransformación de fase I en las que se introducen o exponen grupos polares y en el colon mediante reacciones de biotransformación de fase II, en las que los microorganismos degradan los flavonoides no absorbidos16.
El tema fue ampliamente revisado por Hackett 19 y por Middletown et al20 donde se encuentra abundante informaciónsobre el metabolismo de los flavonoides en animales y en humanos. Una parte importante de los flavonoides ingeridos y metabolizados se excreta por la orina en forma de conjugados
solubles en agua. La conjugación con el ácido glucurónico, sulfatos o glicina, parece tener lugar tanto para los flavonoides como para sus metabolitos procedentes del colon1.
Acción antioxidante y cardioprotectora de los flavonoides El creciente interés en los flavonoides se debe a su amplia actividad farmacológica, por lo que se han descrito efectos protectores en diversas condiciones patológicas incluyendo las cardiopatías. Su acción antioxidante es la más conocida de los
flavonoides, sobre la cual Bors et al.21 hizo una amplia revisión y enumeró los siguientes criterios químicos para establecer la capacidad antioxidante de los mismos:
— Presencia de estructura O-dihidroxi en el anillo B; que confiere una mayor estabilidad a la forma radical y participa en la deslocalización de los electrones.
— Doble ligadura, en conjunción con la función 4-oxo del anillo22.
— Grupos 3- y 5-OH con función 4-oxo en los anillos A y C necesarios para ejercer el máximo potencial antioxidante.
De acuerdo con estos criterios, el flavonoide quercitina, presente en el brócoli, tiene una función antioxidante muy efectiva. Su capacidad antioxidante medida como Trolox es de 4,7 mM, la cual es 5 veces mayor a la demostrada por las vitaminas E y C y tiene una hidrosolubilidad similar a la de la vitamina E1. También se ha observado que la función antioxidante de la quercitina muestra efectos sinérgicos con la vitamina C, porque el ácido ascórbico reduce la oxidación de la quercitina, de manera tal que combinado con ella permite al flavonoide mantener sus funciones antioxidantes durante más tiempo. Por otra parte, la quercitina protege de la oxidación a la vitamina E, con lo cual también presenta efectos sinergizantes1,11.
Los flavonoides retiran oxígeno reactivo especialmente en forma de aniones superóxidos, radicales hidroxilos, peróxidos lipídicos o hidroperóxidos. De esta manera bloquean la acción letal de dichas sustancias sobre las células. En otros flavonoides se ha observado una acción inhibitoria en los procesos de peroxidación lipídica del ácido linoleico o de los fosfolípidos de las membranas, la peroxidación de los glóbulos rojos o la autooxidación de los homogeneizados de cerebro23. Asimismo,
se ha comprobado su capacidad de inhibir in vitro la oxidación de las lipoproteínas de baja densidad (LDL) por los macrófagos y reducir la citotoxicidad de las LDL oxidadas5,24. Adicionalmente se ha propuesto un papel potencial de los flavonoides en reducir la vulnerabilidad del endotelio microvascular a las procesos inflamatorios y oxidativos y ejercer una acción protectora del endotelio25 .
También se ha observado que la quercitina mejora la función contráctil del ventrículo izquierdo y reduce la incidencia de trastornos de la conducción cardíaca en ratas. El proceso se limita al área isquémica, protegiendo la ultraestructura de las arterias coronarias, mejorando la circulación coronaria y previniendo la formación de trombos intravasculares. Por otra parte también se han demostrado efectos vasodilatadores en aorta aislada de ratas, efectos antitrombóticos y disminución de las lesiones de reperfusión del miocardio26,25.
Se reconoce que niveles elevados de LDL y especialmente LDL oxidada son factores de riesgo en la enfermedad arterial coronaria. Ya en 1990, De Whalley et al20 demostraron que ciertos flavonoides eran inhibidores de la modificación de LDL por macrófagos en ratones. Los flavonoides también inhibieron la oxidación de células libres de LDL mediadas por CuSO4.
Parece que los flavonoides actúan protegiendo las LDL contra la oxidación causada por macrófagos, al inhibir la generación de lípidos hidroperóxidos. Así, los flavonoides protegen a las LDL de la oxidación, manteniendo sus niveles por períodos de tiempo más prolongados, y retardando el comienzo de la peroxidación de los lípidos.
Sin embargo, los mecanismos de acción por los cuales los flavonoides inhiben la oxidación de las LDL no están totalmente claros. Se han hipotetizado algunas posibilidades.
La transformación de los flavonoides ocurre en el hígado, por medio de reacciones de biotransformación de fase I en las que se introducen o exponen grupos polares y en el colon mediante reacciones de biotransformación de fase II, en las que los microorganismos degradan los flavonoides no absorbidos16.
El tema fue ampliamente revisado por Hackett 19 y por Middletown et al20 donde se encuentra abundante informaciónsobre el metabolismo de los flavonoides en animales y en humanos. Una parte importante de los flavonoides ingeridos y metabolizados se excreta por la orina en forma de conjugados
solubles en agua. La conjugación con el ácido glucurónico, sulfatos o glicina, parece tener lugar tanto para los flavonoides como para sus metabolitos procedentes del colon1.
Acción antioxidante y cardioprotectora de los flavonoides El creciente interés en los flavonoides se debe a su amplia actividad farmacológica, por lo que se han descrito efectos protectores en diversas condiciones patológicas incluyendo las cardiopatías. Su acción antioxidante es la más conocida de los
flavonoides, sobre la cual Bors et al.21 hizo una amplia revisión y enumeró los siguientes criterios químicos para establecer la capacidad antioxidante de los mismos:
— Presencia de estructura O-dihidroxi en el anillo B; que confiere una mayor estabilidad a la forma radical y participa en la deslocalización de los electrones.
— Doble ligadura, en conjunción con la función 4-oxo del anillo22.
— Grupos 3- y 5-OH con función 4-oxo en los anillos A y C necesarios para ejercer el máximo potencial antioxidante.
De acuerdo con estos criterios, el flavonoide quercitina, presente en el brócoli, tiene una función antioxidante muy efectiva. Su capacidad antioxidante medida como Trolox es de 4,7 mM, la cual es 5 veces mayor a la demostrada por las vitaminas E y C y tiene una hidrosolubilidad similar a la de la vitamina E1. También se ha observado que la función antioxidante de la quercitina muestra efectos sinérgicos con la vitamina C, porque el ácido ascórbico reduce la oxidación de la quercitina, de manera tal que combinado con ella permite al flavonoide mantener sus funciones antioxidantes durante más tiempo. Por otra parte, la quercitina protege de la oxidación a la vitamina E, con lo cual también presenta efectos sinergizantes1,11.
Los flavonoides retiran oxígeno reactivo especialmente en forma de aniones superóxidos, radicales hidroxilos, peróxidos lipídicos o hidroperóxidos. De esta manera bloquean la acción letal de dichas sustancias sobre las células. En otros flavonoides se ha observado una acción inhibitoria en los procesos de peroxidación lipídica del ácido linoleico o de los fosfolípidos de las membranas, la peroxidación de los glóbulos rojos o la autooxidación de los homogeneizados de cerebro23. Asimismo,
se ha comprobado su capacidad de inhibir in vitro la oxidación de las lipoproteínas de baja densidad (LDL) por los macrófagos y reducir la citotoxicidad de las LDL oxidadas5,24. Adicionalmente se ha propuesto un papel potencial de los flavonoides en reducir la vulnerabilidad del endotelio microvascular a las procesos inflamatorios y oxidativos y ejercer una acción protectora del endotelio25 .
También se ha observado que la quercitina mejora la función contráctil del ventrículo izquierdo y reduce la incidencia de trastornos de la conducción cardíaca en ratas. El proceso se limita al área isquémica, protegiendo la ultraestructura de las arterias coronarias, mejorando la circulación coronaria y previniendo la formación de trombos intravasculares. Por otra parte también se han demostrado efectos vasodilatadores en aorta aislada de ratas, efectos antitrombóticos y disminución de las lesiones de reperfusión del miocardio26,25.
Se reconoce que niveles elevados de LDL y especialmente LDL oxidada son factores de riesgo en la enfermedad arterial coronaria. Ya en 1990, De Whalley et al20 demostraron que ciertos flavonoides eran inhibidores de la modificación de LDL por macrófagos en ratones. Los flavonoides también inhibieron la oxidación de células libres de LDL mediadas por CuSO4.
Parece que los flavonoides actúan protegiendo las LDL contra la oxidación causada por macrófagos, al inhibir la generación de lípidos hidroperóxidos. Así, los flavonoides protegen a las LDL de la oxidación, manteniendo sus niveles por períodos de tiempo más prolongados, y retardando el comienzo de la peroxidación de los lípidos.
Sin embargo, los mecanismos de acción por los cuales los flavonoides inhiben la oxidación de las LDL no están totalmente claros. Se han hipotetizado algunas posibilidades.
Primero: podrían reducir la generación o liberación de radicales libres en los macrófagos o podrían proteger al alfa-tocoferol en las LDL de ser oxidados por los mismos radicales libres. Segundo: los flavonoides podrían regenerar el alfa-tocoferol activo donando un átomo de hidrógeno al radical alfa-tocoferil, el cual se forma cuando transfiere su propio OH a un radical para terminar la cadena de la reacción de la peroxidación lipídica. Tercero: los flavonoides podrían secuestrar iones metálicos, tales como hierro y cobre, disminuyendo los radicales libres generados en el medio.
Evidencias preliminares indican que la isoflavona genisteina inhibe la oxidación de las LDL mediada por Cu2+ en función de la concentración y el tiempo27. Sin embargo, dado que algunos flavonoides a concentración de solo 10 mM inhiben completamente la modificación de las LDL en 100 mM de Cu2+,
se percibe que tan solo la quelación de iones metálicos por los flavonoides no podría explicar todos sus efectos. La oxidación de los productos de los LDL inducida por la radiación UV ataca principalmente el núcleo lipídico de las LDL, en contraste a la oxidación celular o a la oxidación mediada por el cobre, la cual primariamente ataca los componentes de la superficie de las LDL28. En otra investigación, dichos autores informaron acerca de la protección de líneas de células linfoides contra el estrés peroxidativo inducido por LDL oxidada usando una combinación de alfa-tocoferol, ácido ascórbico, y quercetina29.
Estos investigadores también mostraron que la citotoxicidad de LDL oxidado podía ser prevenida por flavonoides en dos formas: o bien inhibiendo la peroxidación de los lípidos de las LDL (inducidos por irradiación UV) o por bloqueo a nivel celular la citotoxicidad de las LDL previamente oxidadas30. La
inhibición de la peroxidación de los lípidos de las LDL por los flavonoides se mostró muy correlacionada con la prevención de la citotoxicidad del LDL oxidada.
En la protección de las células por flavonoides polifenólicos, se han propuesto dos líneas de defensa:
1) de los estudios que usaron quercetina o rutina a concentraciones moderadamente altas (IC50, 10–20 mM), hubo inhibición de la oxidación de la lipoproteína y una subsecuente citotoxicidad, y 2) a concentraciones relativamente bajas (IC50, 0,1 y 3 mM), hubo una protección directa de las células contra el efecto citotóxico del LDL oxidado.
Los mecanismos celulares para esta prevención directa de efecto citotóxico del LDL oxidado son desconocidos, pero podrían involucrar los siguientes:
Evidencias preliminares indican que la isoflavona genisteina inhibe la oxidación de las LDL mediada por Cu2+ en función de la concentración y el tiempo27. Sin embargo, dado que algunos flavonoides a concentración de solo 10 mM inhiben completamente la modificación de las LDL en 100 mM de Cu2+,
se percibe que tan solo la quelación de iones metálicos por los flavonoides no podría explicar todos sus efectos. La oxidación de los productos de los LDL inducida por la radiación UV ataca principalmente el núcleo lipídico de las LDL, en contraste a la oxidación celular o a la oxidación mediada por el cobre, la cual primariamente ataca los componentes de la superficie de las LDL28. En otra investigación, dichos autores informaron acerca de la protección de líneas de células linfoides contra el estrés peroxidativo inducido por LDL oxidada usando una combinación de alfa-tocoferol, ácido ascórbico, y quercetina29.
Estos investigadores también mostraron que la citotoxicidad de LDL oxidado podía ser prevenida por flavonoides en dos formas: o bien inhibiendo la peroxidación de los lípidos de las LDL (inducidos por irradiación UV) o por bloqueo a nivel celular la citotoxicidad de las LDL previamente oxidadas30. La
inhibición de la peroxidación de los lípidos de las LDL por los flavonoides se mostró muy correlacionada con la prevención de la citotoxicidad del LDL oxidada.
En la protección de las células por flavonoides polifenólicos, se han propuesto dos líneas de defensa:
1) de los estudios que usaron quercetina o rutina a concentraciones moderadamente altas (IC50, 10–20 mM), hubo inhibición de la oxidación de la lipoproteína y una subsecuente citotoxicidad, y 2) a concentraciones relativamente bajas (IC50, 0,1 y 3 mM), hubo una protección directa de las células contra el efecto citotóxico del LDL oxidado.
Los mecanismos celulares para esta prevención directa de efecto citotóxico del LDL oxidado son desconocidos, pero podrían involucrar los siguientes:
a) prevención de la acción oxidativa de los lípidos de la membrana por reposición de la vitamina E, o regenerándola, como lo hace el ácido ascórbico en el mantenimiento de los niveles de alfa-tocoferol;
b) inhibición de lipoxigenasa, de las que se conoce son estimuladas por peróxidos lípidos y podrían estar involucradas en el estrés oxidativo, como lo sugerido por su rol en la oxidación de LDL en la célula, y
c) inhibición de las enzimas involucradas en transducción de señales.
interchange-newline"> Estos resultados sugieren que los flavonoides de la dieta podrían estar involucrados en la prevención de la aterosclerosis no solo por inhibición de la oxidación del LDL, sino también por incrementar la resistencia celular a los efectos dañinos del LDL oxidado.
Además de lo mencionado anteriormente, también se ha observado actividad vasodilatadora y efecto hipotensivo en varios glicósidos flavonoides extraídos de la cáscara de naranja35.
Adicionalmente, Ning et al36 observaron que la administración de flavona mejoró en forma significativa la recuperación funcional en corazón de conejo reperfundido luego de una isquemia masiva. El efecto del flavonoide en la recuperación postisquémica puede atribuirse a la estimulación del sistema del citocromo P450 y las reductasas que transfieren electrones lo que da una utilidad potencial de los flavonoides como unmedio de aumentar la tolerancia isquémica del miocardio o la resistencia al daño por reperfusión